Chapitres

Exercice 1 : Les électrons et la physique
Le problème posé par la nature des « rayons cathodiques » à la fin du XIXème siècle fut résolu en 1897 par l'Anglais J.J. Thomson : il s'agissait de particules chargées négativement baptisées par la suite « électrons ». La découverte de l'électron valut à Thomson le prix Nobel de physique en 1906.
Le défi pour les scientifiques de l'époque fut alors de déterminer les caractéristiques de cette particule : sa charge électrique et sa masse. Dans un premier temps, Thomson lui-même, en étudiant la déviation d'un faisceau d'électrons dans un champ électrique, put obtenir le « rapport e/me » de ces deux caractéristiques.
C'est cependant l'Américain R. Millikan qui, réalisant de multiples expériences entre 1906 et 1913 sur des gouttelettes d'huile, détermina la valeur de la charge de l'électron.
En 1927, G.P. Thomson, le fils de J.J. Thomson, réalise une expérience de diffraction des électrons par des cristaux.
Actuellement, les valeurs admises de la masse et de la charge de l'électron sont :
me = 9,1093826 x 10-31 kg et e = 1,602176565 x 10-19 C.
Donnée : Constante de Planck : h = 6,63 x 10-34 J.s
Cet exercice comprend trois parties indépendantes, en lien avec les travaux de ces trois physiciens.

1. L'expérience de J.J. Thomson
Lors de ses recherches dans son laboratoire de Cambridge, Thomson conçoit un dispositif dans lequel un faisceau d'électrons est dévié lors de son passage entre deux plaques où règne un champ électrique. La mesure de la déviation du faisceau d'électrons lui permet alors de déterminer le rapport e/me.
L'étude suivante porte sur le mouvement d'un électron du faisceau qui pénètre entre deux plaques parallèles et horizontales P1 et P2, dans une zone où règne un champ électrique supposé uniforme et perpendiculaire aux deux plaques.
À l'instant t = 0 s, l'électron arrive en un point O avec une vitesse horizontale v0.
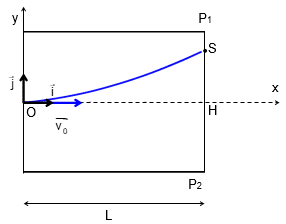
La trajectoire de l'électron dans un repère (O,x,y) est fournie sur L'ANNEXE À RENDRE AVEC LA COPIE.
L'électron de masse me et de charge q = - e, dont le mouvement étudié dans le référentiel terrestre supposé galiléen, est soumis à la seule force électrostatique Fe.
1.1. Sur le document de L'ANNEXE À RENDRE AVEC LA COPIE, représenter sans souci d'échelle et en justifiant les tracés :
- Le vecteur force en un point de la trajectoire de l'électron ;
- Le vecteur champ électrique en un point quelconque situé entre les plaques P1 et P2.
1.2. En utilisant la deuxième loi de Newton, déterminer les équations horaires x(t) et y(t) du mouvement de l'électron.
1.3. Vérifier que la trajectoire de l'électron a pour équation :
\[y = \frac{e \cdot E} {2 \cdot m _ {e} \cdot v ^{2} _ {0}} \cdot x ^{2} \]
1.4. À la sortie de la zone entre les plaques P1 et P2, l'électron a subi une déviation verticale SH comme l'indique le schéma de L'ANNEXE À RENDRE AVEC LA COPIE. On mesure SH = yS = 2,0´10-2 m.
Déterminer, dans cette expérience, la valeur du rapport e/me de l'électron.
Conclure.
Données :
- Longueur des plaques : L = 9,0 x 10-2 m ;
- Vitesse initiale de l'électron : v0 = 2,4 x 107 m.s-1 ;
- Valeur du champ électrique : E = 1,6 x 104 V.m-1 .
2. L'expérience de Millikan
L'objectif de Millikan est de montrer qu'un corps chargé ne peut porter qu'une charge électrique multiple d'une « charge élémentaire ».
Document 1 : Principe de l'expérience menée en 1910 par Millikan
Millikan pulvérise des gouttelettes d'huile chargées par irradiation entre deux plaques planes où règne un champ électrique et les observe à l'aide d'un microscope.
Sa méthode consiste à immobiliser les gouttelettes en augmentant le champ électrique jusqu'à ce que le poids de la gouttelette soit compensé par la force électrostatique.
Millikan parvint ainsi à obtenir une valeur approchée de la charge élémentaire
e = 1,591 x 10-19 C, très proche de la valeur admise aujourd'hui.
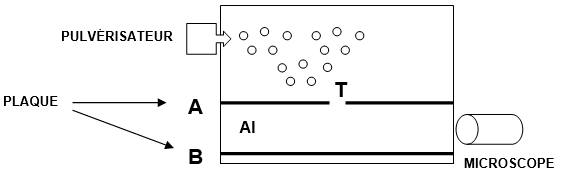
Un pulvérisateur produit un nuage de gouttelettes d'huile chargées négativement qui tombent dans la chambre supérieure du dispositif. Lorsque l'une d'elles passe à travers le trou T, elle tombe verticalement à une vitesse constante v1, son poids étant très vite compensé par la force de frottement exercée par l'air. Lors de cette première étape, la chute verticale de la gouttelette dans l'air en l'absence de champ électrique est observée à l'aide d'un microscope et permet de déterminer le rayon r de la gouttelette qui n'est pas mesurable directement.
Lors d'une deuxième étape, lorsque la gouttelette parvient en bas du dispositif, un champ électrique uniforme est créé entre les plaques A et B. La gouttelette remonte alors verticalement à une vitesse constante v2.
La charge électrique portée par la gouttelette est ensuite déduite des mesures des vitesses v1 et v2.
Lors de l'expérience menée au laboratoire, une gouttelette de masse m et de charge q négative arrive entre les plaques A et B.
La poussée d'Archimède est négligée. La gouttelette étudiée est soumise à son poids P et à la force de frottement f exercée par l'air s'exprimant par la relation :
\[ \overrightarrow { f } = - 6 \cdot \pi \cdot \eta \cdot r \cdot \overrightarrow { v } \]
dans laquelle η est la viscosité de l'air, r le rayon de la gouttelette et le vecteur v sa vitesse.
Données :
- Masse volumique de l'huile : r = 890 kg.m-3 ;
- Valeur du champ de pesanteur : g = 9,8 N.kg-1 ;
- Viscosité de l'air : h = 1,8 x 10-5 kg.m-1.s-1.

2.1. Chute verticale de la gouttelette
2.1.1. Lors de la chute de la gouttelette en l'absence de champ électrique, écrire la relation vectorielle entre la force de frottement et le poids lorsque la vitesse constante v1 est atteinte.
En déduire l'expression de v1 en fonction de η, r, m et g.
2.1.2. La relation précédente peut également s'écrire :
\[ v _ {1} = \frac {2} {9} \cdot \frac {\rho \cdot g \cdot r ^ {2} } { \eta } \]
où ρ est la masse volumique de l'huile.
Déterminer le rayon r de la gouttelette sachant qu'elle parcourt, lors de sa chute, une distance de 2,11 mm pendant une durée Δt =10,0 s.
2.1.3. Afin de faciliter la mesure au microscope, la gouttelette ne doit pas être trop rapide.
En déduire s'il est préférable de sélectionner une grosse gouttelette ou au contraire une petite gouttelette.
2.2. Remontée de la gouttelette
Un champ électrique uniforme étant établi entre les plaques A et B, la gouttelette subit une force supplémentaire Fe verticale et remonte alors avec une vitesse constante v2 atteinte presque instantanément.
On peut montrer que la charge q de la gouttelette est donnée par la relation :
\[ q = - \frac { 6 \cdot \pi \cdot \eta \cdot r \cdot (v _ {1} + v _{2} ) } { E } \]
Plusieurs mesures ont été réalisées pour différentes gouttelettes et rassemblées dans le tableau du document 3.
| Numéro de la gouttelette | Rayon r de la gouttelette (µm) | Vitesse de descente v1 (x 10–4m.s-1) | Vitesse de remontée v2 (x 10-4 m.s-1) | Charge q de la gouttelette (C) |
|---|---|---|---|---|
| 1 | 1,2 | 1,55 | 1,59 | - 6,4 x 10-19 |
| 2 | 1,3 | 1,82 | 1,81 | - 8,0 x 10-19 |
| 3 | 1,5 | 2,42 | 1,35 | - 9,6 x 10-19 |
| 4 | 1,6 | 2,76 | 3,13 | - 1,6 x 10-19 |
| 5 | 1,82 | 2,53 | - 9,6 x 10-19 |
2.2.1. Les gouttelettes n°2 et n°5 du document 3 ont la même vitesse de descente v1 mais des vitesses de remontée v2 différentes.
Déterminer sans calcul le rayon de la gouttelette n°5. Justifier.
Pourquoi leurs vitesses de remontée sont-elles différentes ?
2.2.2. Montrer, à partir des résultats expérimentaux du document 3, que la charge de ces gouttelettes est « quantifiée », c'est-à-dire qu'elle ne prend que des valeurs multiples d'une même charge élémentaire égale à 1,6 x 10-19 C.
2.3. En quoi le protocole de l'expérience effectuée par Millikan diffère-t-il de celui réalisé au laboratoire par J.J. Thomson ?
3. Diffraction des électrons
Davisson et Germer réalisent en 1927 une expérience de diffraction des électrons sur un cristal constitué d'un arrangement régulier d'atomes de nickel. De son côté, G.P. Thomson fait une expérience analogue et réussit également à diffracter un faisceau d'électrons. Il reçoit en 1937 le prix Nobel de physique pour ses travaux, prix qu'il partagea avec Davisson.
3.1. Quelle information sur la nature de l'électron cette expérience donne-t-elle ?
3.2. Dans l'expérience de Davisson et Germer, les électrons avaient une vitesse égale à
4,4 x 106 m.s-1.
Calculer la longueur d'onde de l'onde de matière associée à un électron ayant cette vitesse.
3.3. Quel est l'ordre de grandeur de la distance entre les atomes dans un solide ?
Commenter cette valeur.
Annexes à rendre
Justifications
Exercice 2 : Ondes et électrons
En 1912, Max Von Laue soumet un cristal à des ondes électromagnétiques de courte longueur d’onde, les rayons X. Il découvre ainsi sa structure.
Les solides cristallins présentent au niveau atomique un arrangement parfaitement ordonné et régulier dans trois directions de l’espace. Cet arrangement est caractérisé par la distance a entre deux entités (atomes, ions, molécules). Cette distance est de l’ordre de 0,1 nm. Les solides cristallins ont la propriété de diffracter une onde de longueur d’onde dont la valeur est voisine de la distance a.

1. Diffraction d’un faisceau d’électrons
Les deux représentations ci-dessous montrent la figure de diffraction d’un faisceau de rayons X (à gauche) et d’un faisceau d’électrons (à droite) après passage au travers d’une fine feuille faite de petits cristaux d’aluminium.

1.1 Quelle condition sur la longueur d’onde permet d’observer le phénomène de diffraction ?
1.2 Expliquer en quoi la figure 1 illustre l’hypothèse d’un comportement ondulatoire des électrons.
1.3 Donner la relation de De Broglie qui prend en compte ce comportement ondulatoire des électrons. Quelle est sa signification ?
En 1927, les américains C.J. Davisson et L. Germer apportent la première preuve expérimentale du comportement ondulatoire de particules de masse non nulle.
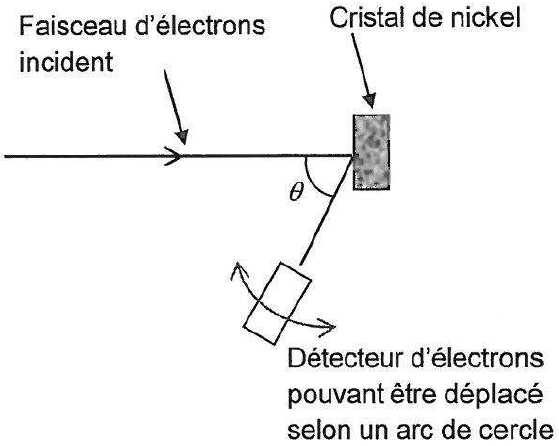
Ils observent ainsi la diffraction d’un faisceau d’électrons de vitesses identiques, par un cristal de nickel.
Le schéma de principe du montage expérimental de Davisson et Germer est représenté ci-contre.
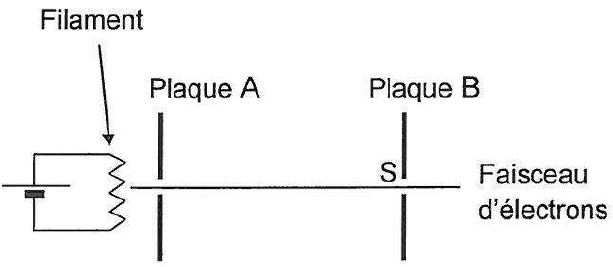
2. Obtention du faisceau d’électrons
Dans l’expérience de Davisson-Germer, des électrons émis sans vitesse initiale par un filament sont accélérés par le champ électrostatique horizontal supposé uniforme qui règne entre deux plaques planes verticales A et B aux bornes desquelles on applique une tension électrique de l’ordre de 100 V.
Données :
- Masse d’un électron : m = 9,11 × 10–31 kg ;
- Charge électrique élémentaire : e = 1,60 × 10–19 C ;
- Constante de Planck : h = 6,63 × 10–34s ;
- La valeur de l’intensité de la pesanteur est supposée connue du candidat ;
- La distance d entre les plaques est inférieure à 1 m ;
- Deux plaques séparées d’une distance d et aux bornes desquelles on applique une tension U créent entre elles un champ électrostatique.
2.1 Montrer que le poids de l’électron peut être négligé devant la force électrique qu’il subit.
2.2 Représenter sur un schéma la force électrique subie par l’électron entre les plaques et le champ électrostatique. Justifier cette représentation.
2.3 Montrer qu’en sortie S du dispositif, l’expression de la vitesse d’un électron est :
\[v _ {s} = \sqrt{ \frac {2 e \cdot U } { m } }\]
Pour ce faire, on pourra déterminer les équations horaires du mouvement d’un électron entre les deux plaques A et B en considérant que sa vitesse est nulle à l’entrée du dispositif.
Les éléments de la démarche, même partielle, seront valorisés.

2.4 Pour observer la diffraction du faisceau d’électrons par le nickel, la longueur d’onde de l’onde de matière associée doit être de l’ordre de grandeur de la distance a caractérisant ce solide cristallin, soit environ 0,1 nm.
2.4.1 Montrer que dans ce cas l’expression de la tension U est donnée par :
\[ U = \frac {h ^ { 2 } } { 2 m \cdot e \cdot \lambda ^{ 2 } } \]
2.4.2 Retrouver l’ordre de grandeur de la valeur de la tension U que Davisson et Germer ont dû choisir pour leur expérience.
3. Une application technologique du phénomène : le microscope électronique
S’appuyant sur les résultats de Davisson-Germer, deux chercheurs allemands (E.Ruska et M.Knoll) ont conçu en 1931 un prototype de microscope électronique utilisant un faisceau d’électrons accélérés par une tension U de l’ordre de 100 kV.
Sachant que la résolution (plus petite distance séparant deux objets que l’on peut distinguer) d’un microscope optique ou électronique est proportionnelle à la longueur d’onde du rayonnement utilisé, expliquer en quelques lignes une raison qui a pu motiver les chercheurs à se lancer dans l’élaboration d’un microscope électronique.






















Si vous désirez une aide personnalisée, contactez dès maintenant l’un de nos professeurs !